前言:近年来,我国医疗器械行业迎来前所未有的发展良机,我们认为未来十年是国产创新医疗器械的黄金发展时期。从内因来看,随着我国医药、机械、电子等学科的快速发展,国产医疗器械不断实现技术创新,逐步突破多项技术壁垒;在配套产业链方面,我国已经形成多个专业化产业集群,供应链上游原材料国产比例持续提升,为企业控制成本、扩大生产规模创造了条件。从外因来看,在医保控费、分级诊疗以及国家对于国产创新器械加大支持力度的政策环境下,国产医疗器械有望加速进口替代以及行业集中度提升,国产龙头有望借机实现逆袭;资本市场对医疗器械的投资意向上升,大量资本流入医疗器械行业,形成了我国较为活跃的医疗器械投融资以及并购市场,驱动行业加速创新与升级。从估值方法看,医疗器械板块中优质的产品管线,也会类似于创新药,开启 pipeline 估值法,器械估值体系有望重塑。
毋庸置疑,从 2016 年开始,市场上对于创新药的研究层出不穷,投资者对于创新药的临床试验、审批、定价、招标等流程了解比较充分;然而市场上几乎没有对于医疗器械的临床试验、专利、审批、定价与招采等流程较系统的研究,我们发表这篇深度报告,旨在对于医疗器械的上述流程进行全面阐述和系统性梳理,以便更好地把握医疗器械领域的投资机会。

1、医疗器械注册审评流程追溯
1.1、医疗器械注册流程(略)
在我国,医疗器械的注册流程可主要分为两个阶段:一是注册申报资料准备阶段,主要包括分类、注册检验、临床评价等环节;二是审评审批阶段,主要包括注册申报受理、审评审批、发补、拿证等。医疗器械获批上市后,还可能需要进行注册延续、注册变更等过程。
1.2、医疗器械临床试验(略)
医疗器械临床试验是指在经资质认定的医疗器械临床试验机构中,对拟申请注册的医疗器械在正常使用条件下的安全性和有效性进行确认或验证的过程。由于器械与药品之间差异巨大,其临床试验与药物临床试验存在诸多不同。
1.3、创新医疗器械审评审批(略)
随着我国医疗器械行业快速发展,企业创新活力不断提高,审评审批制度改革也在持续推进。但总体来看,我国的医疗器械依然面临着创新支撑不足的困境,产品与国际先进水平仍有不小的差距。为了进一步支持我国产业发展,激发医疗器械企业的创新潜力,满足实际临床中的不同需求,我国于 2014 年 3 月 1 日起施行《创新医疗器械特别审批程序(试行)》,针对创新型医疗器械制定了优先审评审批的方案。2018 年 12 月 1 日,国家药品监督管理局在广泛征询了各方意见后,修订并开始实施新的《创新医疗器械特别审查程序》,进一步完善了适用情形、细化了申请流程、提升了创新审查的实效性,并明确对创新医疗器械的许可事项变更优先办理,为我国的医疗器械产业发展提供了有力的政策支持。
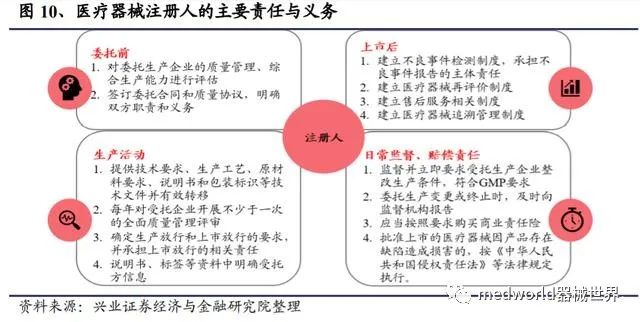
1.4、医疗器械上市许可持有人制度
上市许可持有人(Marketing Authorization Holder,MAH)制度又称“注册人制度”,是一种将上市许可与生产许可相分离的管理模式。在这种模式下,上市许可持有人可以将产品的生产委托给其他专门的生产商,而产品的安全性、有效性等质量保障则均由上市许可持有人负责。由此,通过将上市许可和生产许可进行“解绑”,可以有效抑制医疗器械制造企业的低水平重复建设,提高新型产品研发和生产的积极性,推动委托生产行业快速发展,从而在整体上达到促进我国医疗器械行业繁荣发展的目的。
医疗器械 MAH 制度的目标主要有三点:一是构建一个自始至终为医疗器械的产品质量承担管理义务的责任主体;二是解除医疗器械产品上市许可和生产许可的捆绑关系,让医疗器械 MAH 成为疏通产品注册与生产管理壁垒的主体;三是优化医疗器械行业资源的分配,刺激行业研发投入增加,为高技术含量的新产品研发扫除障碍,从而推动整个行业的创新发展。
医疗器械 MAH 制度的关键内容包括:首先,允许科研机构和研发人员作为注册申请人,提交医疗器械临床试验申请和上市许可申请,取得医疗器械注册证的申请人即转变为医疗器械注册人,也就是医疗器械 MAH。其次,医疗器械 MAH 具备相应生产资质的,既可自行生产,也可委托生产。持有人不具备生产条件的,可以直接委托具备资质的企业生产产品。第三,在医疗器械委托生产中,如果受托方不具备生产资质,可凭委托方的注册证办理生产许可。第四,医疗器械注册人可委托多个受托方进行生产。
在医疗器械 MAH 制度实施之前,上市许可一般只颁发给具有医疗器械生产资质的企业,研发机构和科研人员并没有独立获得上市许可的机会。在医疗器械委托生产的过程中,一般规定只能指定一家生产企业作为受托人。也就是说,医疗器械从产品注册到委托生产这一过程中,注册与生产是深度捆绑的,这导致行业资源流动受限和社会生产分工受阻,最终影响行业整体的健康发展。
MAH 制度对我国医疗器械企业的影响
允许研发机构和科研人员申请上市许可。MAH 制度改写了过去医疗器械产品注册和生产许可“相互捆绑”的历史,允许符合条件的医疗器械研发机构、科研人员、医生等成为注册申请人,单独申请医疗器械注册证,并委托有资质和生产能力的企业进行生产。持有人制度还将改变我国原有制度下,科研人员只能通过技术转让或隐名持股获得短期利益、隐名利益的尴尬局面,极大地鼓励研发机构和科研人员从事医疗器械创新,有效激发市场活力,加快我国由医疗器械生产大国向创新大国的转变。
研发型企业专注研发环节,降低企业成本。据统计,我国医疗器械相关企业共有4 万多家,其中生产企业约 1.6 万家,且 90%以上为中小型企业,技术含量较低,年产值过亿的企业不足 400 家。医疗器械 MAH 制度的推出可有效解决初创企业早期面临的资金有限、生产人员缺乏等困境,让创新企业、研发企业专注于产品的研发环节,把生产环节开放给服务企业,在加强创新的同时降低企业成本。例如,采用外包方式生产二类(气腹机等)医疗器械的企业三年便可节约费用近 1000万元,同时还可以大幅缩短产品的上市周期,实现新产品的快速产业化,使企业更具市场竞争力。
优化资源配置,产业链整体受益。数据显示,我国中小医疗器械生产企业的工厂使用率只有 5%-10%,造成大量资源浪费。施行 MAH 制度后,医疗器械研发机构和科研人员可以选择自行生产或委托生产,有效避免企业低水平重复现象,改善同一品种多家许可、多家竞争的局面,提高资源的使用效能。此外,MAH 制度还可促进医疗器械行业的专业化分工进程。创新型企业专注源头创新,CRO 辅助企业研发,CMO 进行产品生产落地,医疗器械服务企业也可加速进行市场布局。可以预计,持有人制度全面实施后,我国医疗器械产业将快速进入分化与重组的时期,产品产业集中、创新集聚的步伐将进一步加快,市场竞争、生态优化的活力将进一步迸发。
落实企业责任,强化全程管理。在 MAH 制度下,上市许可持有人对医疗器械质量的全生命周期负责,这种明确而严格的责任制度将有效强化持有人“从实验室到医院”管理责任的全面落实。同时,医疗器械管理的直接对象将从多元主体转移到单一主体,管理的核心内容将从准入资格管理转移到体系能力管理,管理的基本方式将从传统管理转移到现代管理,我国的医疗器械行业将进入全新的智慧管理时代。
1.5、我国器械注册审批与国外差异(略)




2、医疗器械定价与支付方式分析
2.1、国内医疗器械的定价与支付方式(略)
我国医疗器械定价及管控机制
在当下,我国医疗器械市场存在两级分化现象。低端市场生产企业众多,竞争异常激烈,低端医疗器械主要由市场自主定价,企业结合生产成本、市场需求和竞争情况确定产品价格,与药品市场调节定价方法类似。国内高端医疗器械市场,尤其是大型器械、精密器械等,有 70%左右依赖进口,行业的对外依存度较高。所以,高端医疗器械的市场定价受产品到岸价、外贸、流通等众多环节和因素的影响。在我国医疗器械市场潜力巨大、本土研发不足、跨国企业技术引领等形势共同作用下,行业的定价机制既不同于美国的基于市场规律的定价,也不同于英、德的基于政府管制或医保制度的定价,需要综合考虑多种因素制定一套定价策略。
目前我国医疗器械尚不在政府定价范畴内,生产经营企业(供应商)可以自主定价,政府对医疗器械价格的管理属于中间管理,主要体现在集中采购或招标采购以及通过医疗服务项目打包收费上,同时对植 (介) 入类医疗器械进行价格监控。与药品定价机制、医疗服务定价机制较为完备的现状相比,医疗器械定价机制尚不健全。
从国内来看,浙江省和上海市是我国医疗器械价格管控的典型模式。浙江省从医院使用的角度来确定收费目录,省集中采购招标办根据收费目录内的医疗器械进行招标,同时医保部门仅依据收费目录内的医疗器械进行医保支付。整个流程有效地避开了医疗器械品种繁杂、无法统一管理的难点。上海市则充分利用行业组织的“专业性、社会性”等特点,将收费目录内六类医疗器械价格的申报、审核权限以法律条文的形式,明确下放至上海市医疗器械行业协会、上海市医药商业协会,不仅有效提升了医疗器械价格管理的科学性,也提高了价格管理的工作效率。
我国医疗器械价格形成方式
医疗器械价格的形成一般要经历三个环节:生产、流通和医疗机构使用。生产环节中,国产及进口医疗器械产品的出厂价格(到岸价)形成机制无明显差异;流通环节中,目前进口医疗器械的培训、运输、售后服务等费用主要由医疗器械生产企业或总经销商负担,而这些环节的相关费用已成为部分利益相关者牟取暴利的手段;使用环节中,国产及进口医用检查治疗设备均以检查费的形式来体现其价格,医疗器械价格管理主要通过医疗服务项目打包收费或加价率(额)控制两种方式:一是植(置)入类医疗器械和少数特殊材料,允许在医疗服务项目外单独向患者收费;二是低值卫生材料,作为医疗服务成本的一部分,纳入医疗服务项目中打包收费,不单独计价。
根据 2009 年广东省物价局对医用耗材价格的专项调研结果显示:生产环节,部分医疗器械的实际平均出厂价比其单位产品成本高 70%以上;流通环节,医疗器械从出厂(或进口)到医疗机构销售给患者,平均加价 2-3 倍,个别产品甚至多达十几倍;使用环节,广东医药价格协会为期三年的跟踪调查显示:医用耗材费用在住院患者医疗费用中的平均占比接近 20%,且逐年增加。
目前来看,我国医疗器械的定价机制基本上属于政府管理下的,由经销商、医院、医生等利益相关主体影响的市场定价机制。由于医疗器械产品质量及营销模式不同,不同生产企业、不同品规的高值医用耗材销售价格差异大。此外,医用耗材量价挂钩特征明显,部分耗材价格因医院供货量不同,供货价格存在 10%-20%的差异。以体外诊断仪器及试剂的定价为例:

我国医疗器械支付方式
使用环节中,国产及进口医用检查治疗设备均以检查费的形式来体现其价格。患者在医院进行影像学检查(X 线造影、磁共振和 CT 检查诊断等项目),或者使用体外诊断试剂进行检测时,支付的费用是医院统一收费定价再扣除医保报销部分。目前医院的收费定价各省市不尽相同,根据内部实际情况确定。

2.2、海外医疗器械的定价与支付方式
海外医疗器械定价及管控机制
美国是市场化主导的国家,且其未建立全民医保,因此,美国对医疗器械产品价格采取以市场化定价机制为主、卫生部门进行适度调节的思路,最终产生了按产品价值与市场竞争定价法、政府部门通过市场手段影响采购价格的价格形成机制。
英国的医疗卫生体制为政府主导型,英国卫生服务系统(NHS)负责管理医疗卫生的相关事务,医疗服务和药品、器械的支付方和提供方都是有政府直接提供经费、控制和经营。因此,英国主要通过政府采购的方式和过程影响器械产品的价格形成。
德国拥有强大的社会保险制度,其在历史发展过程中形成了强制型社会健康保险辅以商业保险的医疗保险制度。德国政府在医疗器械的招标采购过程中仅负责制度和法规设计,德国社会保险制度由上千个疾病基金负责管理,因此,其医疗器械定价主要由社会保险部门来约束。
医疗器械价格形成过程有诸多利益集团参与,不同利益集团的角色、资源、影响力等方面都存在显著差异,他们最终的行为倾向会对医疗器械价格的确定产生重要的影响。

海外控制医疗设备和耗材费用的过快增长以间接管理为主。各国控制医疗设备和耗材费用的过快增长主要有以下几种方法:(1)通过第三方组织制衡,如美国通过保险公司和卫生保健管理组织(MCO)批量折扣、使用目录进行制衡;(2)通过集中采购降低采购成本,如英国集中采购在控制成本的同时注重产品的改进和创新;(3)通过医保控费制度进行制衡,如德国统一规定部分医疗器械的最高报销限额;(4)通过制定明确的价格法规进行管理,如加拿大采取比价法制定器械价格;(5)通过制定大型医用设备的配置、审批制度制衡大型设备的支出成本,如西班牙和比利时,建立了根据人口比例采购大型医疗设备的审批制度。
海外医疗器械支付方式
医疗器械的支付也不同于一般的消费品,很多时候使用者并不是医疗器械的实际支付者(常常由医保来支付,也可能是医院来支付)。目前全球比较常用的医疗费用支付方式有:按项目付费、按服务单元付费(应用较少)、按人头付费、总额预付、按病种付费等,各种付费方式都有其优缺点。
按人头付费(Capitation)是指医疗保险组织根据医疗机构的规模、技术、服务对象的特点等情况,按照事先确定的每个服务对象(人)的支付标准及所服务的人口数,向该医疗机构预先支付一笔固定费用,医疗机构则负责向目标人群提供相应的医疗服务,如果医疗机构提供服务的总成本超出了支付总额,则经济风险由医疗机构承担,这也是一种预付费方式,如英国的全科医生都是采用这种方式。
总额预付(Global Budget),是指在年度医保基金收入预算确定的情况下,对医保基金总支出的计划安排,即医疗保险机构根据某一区域以前年度参保人数、就诊患者数量、次均卫生费用水平,综合考虑就诊患者数量增长、通货膨胀、技术进步等因素确定下一年的费用预算总额,然后将费用分配到不同的医院及科室,医疗机构在预算费用内提供医疗服务的一种支付方式,如果实际发生费用超支,超支部分由医院自己承担,以保证医保费用支出控制在合理的增长范围(一般不大于医保基金收入的增长水平)。总额预付是过渡阶段的支付方式,例如德国 70 年代开始实施总额预付,2003 年后逐步过渡到按病种付费。
按病种付费,即 DRGs( Diagnosis Related Groups)是当今世界公认的比较先进的医保支付方式之一,称为诊断相关分组,是一种病人分类方案,是专门用于医疗保险预付款制度的分类编码标准。它根据病人的年龄、性别、住院天数、临床诊断、病症、手术、疾病严重程度,合并症与并发症及转归等因素把病人分入 500-600 个诊断相关组,在分级上进行科学测算,给予定额预付款。也就是说 DRGs 就是医疗保险机构就病种付费标准与医院达成协议,医院在收治参加医疗保险的病人时,医疗保险机构就该病种的预付费标准向医院支付费用,超出部分由医院承担的一种付费制度。目前世界上共有 30 多个国家已经实施或正在实施按病种付费制度,应用比较成熟的国家主要有美国、英国、德国和澳大利亚等。

3、医疗器械招标采购方式及流程梳理
3.1、我国设备招标采购方式
公立医院设备采购资金的性质和来源
根据《财政部关于将按预算外资金管理的收入纳入预算管理的通知》(财预[2010]88 号文件)规定和现行《政府收支分类科目》的划分,现在公立医院不再有“预算外资金”这一概念,公立医院所有资金都纳入预算管理,都属于财政性资金。公立医院使用自筹资金和财政拨付资金采购政府采购目录内和政府采购目录外限额标准以上的货物适用于《中华人民共和国政府采购法》及其实施细则;公立医院采购由国家发改委部门单独立项审批的工程及与工程直接相关的货物,采购预算在 100 万元及以上项目招投标的,适用《中华人民共和国招标投标法》及其实施细则。
在医疗设备实际采购中,公立医院资金来源具有多样性。在公立医院设备采购的资金中,除了医院的自筹资金以外,政府财政为推进医院建设和医疗改革也会有专项设备采购的资金拨款。此外,在医院的科研设备的采购中也有横向的设备购买专项经费。


公立医院设备采购的方式
我国公立医院医疗设备的采购主要有政府采购和自行采购两种类型:
公立医院政府采购
公立医院政府采购的主要方式有公开招标、邀请招标、竞争性谈判、询价和单一来源采购等,公开招标是政府采购的主要采购方式。各省市公立医院政府集中采购目录和标准由所在地政府颁布,集中采购目录是公立医院编制年度政府采购预算、申报政府采购计划的依据,也是财政、纪检监察、审计等部门实施监督检查的主要内容。
政府集中采购目录以外、限额标准以上的为分散采购。分散采购可以用招标采购,也可以用非招标采购,但达到公开招标的限额标准必须按照国家法律规定进行公开招标,特殊情况不能采取公开招标的,必须经当地财政部门批准同意后才能使用其他采购方式。
公开招标:是指采购方作为招标方,事先提出采购的条件和要求,以向全社会公开发布招标公告的方式邀请众多医疗器械厂商或代理商参加投标,然后由采购方按照规定的程序和标准一次性的从中择优选择交易对象,并与提出最有利条件的投标方签订协议的过程。当前很多医疗设备的采购,都是选择的这一种招标方式。
邀请招标:根据《政府采购法》符合以下 2 种情形之一的可以采用邀请指标法:(1)具有特殊性,只能从有限范围的供应商处采购的;(2)采用公开招标方式的费用占政府采购项目总价值的比例过大的。
竞争性谈判:是指采购人或者采购代理机构直接邀请三家以上供应商就采购事宜进行谈判的方式。根据《政府采购法》符合以下 4 种情形之一的可以采用竞争性谈判:(1)招标后没有供应商投标或者没有合格标的或者重新招标未能成立的;(2)技术复杂或者性质特殊,不能确定详细规格或者具体要求的;(3)采用招标所需时间不能满足用户紧急需要的;(4)不能事先算出价格总额的。
询价采购:主要指通过询价的方式,直接向 3 家以上的供应商询问报价,并进行横向比较,使要采购的器械价格具有竞争性的采购方式。根据《政府采购法》,采购的货物规格、标准统一、现货货源充足且价格变化幅度小的政府采购项目适用该方式。
单一来源采购:根据《政府采购法》符合以下 3 种情形之一的可以采用单一来源法:(1)只能从唯一供应商处采购的;(2)发生了不可预见的紧急情况不能从其他供应商处采购的;(3)必须保证原有采购项目一致性或者服务配套的要求,需要继续从原供应商处添购的,且添购资金总额不超过原合同采购金额 10%。

公立医院自行采购
政府集中采购目录以外、限额标准以下的货物、服务和工程的采购为公立医院零星采购或称自行采购。各公立医院对货物的自行采购均制定了各自的采购管理办法,建立了相应的采购管理机构。总体上,医院大型设备大多由公开招标方式采购,而小型设备多由医院自行组织采购。
医疗设备采购具体流程(略)
3.2、我国耗材招标采购方式
我国耗材招标采购方式总述
从耗材采购的模式来看,带量采购+阳光挂网+GPO 等几种方式并存。从集采的耗材种类来看,2019 年不仅较多省份落地高值耗材带量采购,还有部分省市对于低值耗材,甚至 IVD 试剂也推行带量采购。

阳光挂网采购
高值医用耗材产品通过省采购平台集中挂网,医疗机构通过省采购平台阳光采购。多数情况下采购主管部门会给出参考限价,要求医院采购不得高于限价,在此基础上医院与企业直接议价采购。省级挂网价逐渐成为地区入市的“门槛”,真正拥有定价权的是医疗机构、地市、医联体等主体。阳光挂网采购可以规范医用耗材的采购全过程行为,寓管理、监督于一体。国家卫生计生委对各地医院所需高值医用耗材按照医院采购目录,以省(区、市)为单位实行集中挂网阳光采购。各省(区、市)根据实际情况,研究确定高值医用耗材阳光挂网采购实施方案,但要求及流程基本相似。以湖南省 2017 年发布的高值医用耗材阳光挂网采购实施方案为例进行介绍。
集团采购联盟(GPO)
医疗耗材的采购最初是医院自行采购为主,随着医改的进行,国家也在大力推动以省(区、市)为单位的医用耗材集中采购工作。在省采购平台(阳光采购平台)基础上,根据采购联盟会员单位临床需求,利用“量价挂钩、款价挂钩”的市场机制,通过订单合并,形成 GPO“团购价”。医用耗材采购联盟模式的出现打破了以往医用耗材以医院自行采购的传统模式,使耗材采购价格更加公开透明,在药品之后,医用耗材的采购价格也将会不断创下新低。2019 年 7 月,江苏省发布的《关于推进医用耗材阳光采购的实施意见(试行)》中提出要推进医用耗材分类采购。
西部联盟
由陕西省发起的西部联盟,现在已发展为现在的 15 省际联盟(陕西、内蒙古、宁夏、甘肃、青海、新疆、湖南、黑龙江、吉林、辽宁、广西、贵州、海南、新疆建设兵团、山西)。西部省区药械采购联盟将实现目录与价格共享,动态调整、价格联动,主要是希望在实现耗材集中采购数据互联互通、资源共享的基础之上,再进一步推动跨区域的价格联动和联合采购,以进一步降低医用耗材的虚高价格。第一阶段,西部各省区分别提供现有高值医用耗材的基础数据,实现高值医用耗材基础数据的共享;第二阶段,制定统一的编码标准,确定共同维护和上传机制,确保数据库基础数据安全有效,西部各省区根据各自工作需要,随时调用共享数据库信息,实现各省区高值医用耗材基础数据库数据的统一,资审及价格等信息互联互通。2017 年陕西省分三批完成 13 大类高值耗材全国最低价限价采购,价格最高降幅 98.7%,平均降幅 18.37%。为了扩大效应,还提出了跨省开展医用耗材采购数据共建共享,并形上述省际耗材采购联盟,以数据为基础,与各省区联合议价,对挂网采购的高值医用耗材价格,每半年进行一次大调整;在低值耗材(含试剂)挂网政策出台后,湖南省郴州市、长沙市开始跟进。
京津冀采购联盟
2016 年,北京市、天津市和河北省共同签署了《京津冀公立医院医用耗材联合采购框架协议》,三地实现“一个平台、协同联动、阳光透明、网上采购”,进一步降低耗材虚高价格。2019 年 11 月,京津冀 3 省市联合发布《京津冀医用耗材联合带量采购工作意见的通知》,辽宁、吉林、黑龙江、山西、内蒙古、山东省也表示要积极跟进,参与开展联合采购,建立以京津冀合作为基础的北方采购联盟,形成“3+6”联合采购新模式。2020 年 5 月 18 日,京津冀及黑吉辽蒙晋鲁医药联合采购办公室(3+N 集采联盟)对议价组人工晶体开展议价谈判工作,本次集采共选定了 53 组目录,共 172 个产品,第一轮竞价、第二轮议价谈判,其中有 25 个产品竞价成功,19 个产品议价谈判成功。与联合采购地区医疗机构原采购价相比,第一轮竞价的平均降幅为达 54.21%,最高降幅为 84.73%,谈判降幅官方尚未发布数据,根据初步估算,平均降幅可达 10%-30%。
“沪苏浙皖闽”的华东四省一市联盟
2016 年 11 月,上海、江苏、浙江、安徽、福建这四省一市的代表共同签署《沪苏浙皖闽四省一市建立综合医改联席会议制度协议》,明确将在药品耗材采购、医保支付、医疗服务价格改革、人事薪酬、健康产业发展等方面开展政策协同。2017年 5 月,“沪苏浙皖闽”四省一市综合医改联席会议在上海召开,对四省一市药品和医用耗材联合采购工作方案等进行了研究讨论。会议明确,要推广浙江省、宁波市医用耗材带量采购的成功经验,选择 1-2 类用量大、价格高的医用耗材品种,实行四省一市联合采购,提高采购集中度,压缩虚高价格。所谓“三步评审法”就是:(1)第一步是供应商资质入围由计算机决定:对供应商资质设立若干审核要素,赋予相应的分值,由计算机对供应商资质要素进行评分,按得分从高到低确认入围名单,入围企业不超过 10 家;(2)第二步品牌遴选由专家投票决定:随机抽取 25 名临床专家,各专家独立对资质入围品牌进行投票,按按得票多少遴选价格谈判的入围品牌,入围品牌不超过 5 个;(3)第三步是成交与否由价格决定:价格谈判专家按同质低价、降价幅度、价格谈判结果满意度三要素进行现场议价。议价采用“多轮报价、逐轮淘汰、现场公布”的方式,确定成交产品。这三个步骤环环相扣,又相互独立,保证入围企业均为产品质量可靠、信誉良好、供货及时,同时又最大限度地降低采购价格。
三明采购联盟
福建省三明市率先开展了医药、医疗、医保三医联动的公立医院改革。通过以医保支付为基础的药品联合限价阳光采购,“两票制”的尝试,压低药价,压缩回扣空间,调控力度可谓空前,短时间内基本达到了药品量价齐降的目的。由于三明联盟“量价齐下”的特点,在降低医疗费用、提高医院业务性收入方面取得了“显著成绩”,受到了国家高层、有关部门和医药卫生界的关注及肯定,而因此被推广至全国的医改模式。2020 年 1 月,黑龙江省鸡西市加入三明联盟,联盟成员已达到了 54 个,涵盖了 16 个省份(自治区)。联盟内平台共享、目录共享、价格共享、资源共享,充分发挥采购联盟的协同效应。
带量采购
国家层面的医用耗材集中采购政策最早可追溯至 2000 年国务院体改办等八部联合发布《关于城镇医药卫生体制改革的指导意见》,意见提出要进行药品集中招标采购工作试点,开启了我国医药行业集中采购的先河。根据中国医疗器械行业发展报告,可将 2000 年以来医疗器械集中采购的发展历程分为四个阶段,各个阶段都有相关国家政策出台。

带量采购的品种选择
从带量采购的耗材品种定位来看,不是所有耗材都适合带量采购,也不是所有耗材都是暴利和价格虚高,近 5 年来各地的招采工作还是“功不可没”的,有些类别行业虚高价格已经压缩了很多。
解决方案:
1) 根据采购物品的 80/20 法则,采用重点管理的办法进行采购。通常数量或种类为 80%的采购物品只占总价值的 20%,而剩下数量为 20%的物品则占有 80%的价值。
2) 应充分考虑耗材的行业属性,按要素特点对产品进行筛选,应当选择同类产品间差异度不大、医生偏好少,产品风险小、市场供应风险小的品类。高值耗材大都是用于危急重症的治疗,耗材的疗效与术者技术密切相关,医生技术是在实践中长期练习积累形成的,术者与器材配合至关重要,应当尽量尊重医生习惯,和企业产品推广的价值。国外通过医院卫生技术评估(Hospital-Based Health Technology Assessment,HB-HTA)来解决这一问题,先对产品的特点进行评价,并在此基础上确定产品的选择和价格。根据当下国内临床技术的成熟度,心脏介入、骨科、眼科、血液透析等耗材相对来说适合带量采购。
带量采购“量”的确定方式
根据目前安徽、江苏等地的带量采购试点方案,各地的“量”的确定方式不同。总体来看,有以下三种方式:
1)市场份额:该种集采方案是给出市场份额的方式,即区域内或医院集团年度使用份额百分比。例如安徽省参加带量采购的耗材种类为占 2018 年度省属公立医疗机构骨科植入(脊柱)类和眼科(人工晶体)类高值医用耗材采购量 70%、90%的产品。这种方式操作相对简单,市场开放,对于企业也比较公平,较有价值。
2)企业历史用量或比例:该种集采方案是给出区域内或医院内某厂家自身产品历史用量额或者比例。例如南京的第二轮谈判是从械企出发,挑选在医院有一定使用量的一家械企进行谈判,方案提出保证该企业去年在联盟地区医院采购量的70%。这种方式下,市场开放性差、公平性差,通过行政手段干预市场竞争,在该种方式下,医院可能虚假报量,适用产品销量不稳定或独家企业,价值含量较低。
3) 市场真实量:该种集采方案是给出真正一个区域或医院集团的市场量,有具体数值。这种方式需要医疗机构和医生的支持(非行政命令),给出真实需求量。市场开放,公平竞争,是带真正的市场的量,价值含量高。

带量采购市场参与主体的积极性
带量采购需要充分调动市场交易主体--医院和企业的积极性。从医院和医生的利益方面,应当充分重视产品性能与临床需求关系,从产品卫生经济价值出发,考虑医生、患者选择权利,带量的规模不宜过大,给医院、医生、特殊病患留出一定空间,耗材采购实行带量采购+阳光挂网+GPO 结合的方式。从企业的利益和长远发展考虑,医用耗材行业科技含量高,企业研发投入大、市场培育周期长,器械创新性强,各厂家技术各有特点,单纯压缩市场价格会有很多不利后果,会打击企业研发创新产品的积极性。
因此,选择同类产品间差异度不大、医生偏好少,产品风险小、市场供应风险小的品类;带真正市场的量,尽量不是企业自身市场历史用量,公平竞争,减小干预市场;理顺机制,充分发挥医疗机构和企业主动参与带量采购的积极性,调动医生使用的积极性,保障货款,附加优待,如推行医保支付价等政策均是带量采购能够成功实施的先决和辅助条件。

我们认为未来高值耗材带量采购将逐步常态化。从耗材集采的地区来看,中央与地方权责逐步明晰,多数耗材集采仍将以地方为主,中央部门负责特殊类别品种集采,地方部门可以做全部耗材品目集采;医用耗材采购中有望应用医院卫生技术评估方法;带量采购+提升医疗服务项目收费+DRGS+医用医保耗材目录等政策多管齐下,改变耗材行业利益格局。

高值耗材带量采购对行业的影响:游戏规则重构,行业面临洗牌
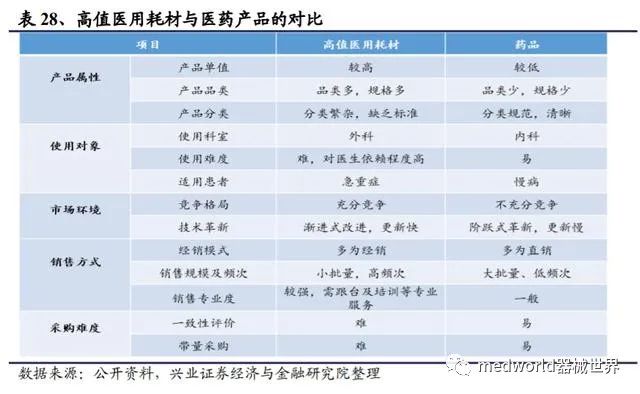
不同于药品带量采购,耗材带量采购对于国产龙头企业机遇大于风险。高值耗材和药品由于在产品属性、销售方式及采购模式上存在诸多不同:
1) 产品分类:与药品规范清晰的分类不同,高值耗材范围非常广,分类复杂,缺乏统一的行业标准和编码体系;
2)使用科室:耗材使用科室多与外科相关,而药品多为内科使用;
3)使用难度:耗材的使用对于术者依赖程度高,使用过程复杂,特异性强;药品处方开具后对医生几乎无依赖,使用过程简单;
4) 适用患者:耗材多适用于急症、重症手术,药品适用患者多为慢病;
5)市场环境:药品多数为竞争充分,而耗材多数不充分,同时耗材用量相对小,更新换代快,药品用量巨大,换代慢;
6)销售方式:与药品多为直销不同,耗材多为经销,由于高值耗材型号众多,专业要求更高,需要渠道商对于部分高值耗材承担培训、调试、维修等服务;
7)采购方式:药品相对简单,带量容易;耗材较为复杂,不同厂家间产品差异性明显,且难以进行一致性评价,带量采购难;
总体来看,医疗器械与药品产品属性不同,没有“原研”和“仿制”的区别,各类器械规格参数众多,难以进行“一致性”评价,质量分级只能通过临床数据、医生评价以及产品材料进行质量区分;而且一致性评价需要较长的周期,而耗材通常来说生命周期只有两年左右,厂家自己针对产品的频繁换代可能会导致一致性评价还没做完,产品就退市了。所有的高值耗材中只有冠脉支架差异是最小的,所以江苏省首先选择冠脉支架试点集采。
带量采购的目的是挤出耗材价格中虚高的销售费用,生产企业最终承担的价格降幅在于渠道的利润空间,如果渠道利润空间较大,对于生产企业的影响则微乎其微。耗材带量采购中标的几家企业能够独享该省(市)公立医院超过 70%的市场份额,有利于行业集中度的提升、龙头企业市占率的扩大。随着高值医用耗材带量采购在全国更大范围内铺开,未中标厂家的市场份额将被进一步压缩,同时由于中小型耗材生产企业往往产能相对有限,且在两票制下,经销商的角色转为配送商,生产厂家需要在全国各地建立多个外仓,以快速响应医院需求,而外仓的建仓和配套相关费用对小公司而言是一个壁垒;两票制后,行业账期普遍拉长,小公司不具有资金和成本优势,难以与大型企业相抗衡。通过优胜劣汰的机制,推动高值医用耗材行业向集约化、规范化、健康化的方向发展。

从长期来看,我们认为耗材带量采购有利于行业集中度的提升,未来符合卫生经济学、具有明确临床诊疗价值的耗材有望受益,国产耗材由于具有性价比高优势,有望逐步抢占进口的市场份额;拥有自主创新能力、业务多元化布局,或是单一产品具有高技术含量和高附加值,在差异化竞争中具有明显的优势的国产龙头企业有望在行业洗牌中受益。
3.3、国外医疗器械的采购方式(略)
世界卫生组织(WHO)2016 年对全球 173 个国家医疗器械采购政策的梳理显示,110 个国家在国家层面采购医疗器械,占 63.58%;74 个国家拥有国家采购或报销医疗器械清单,占 42.77%;85 个国家具有国家医疗器械采购指南,占 49.13%;86 个国家具有支持采购或捐赠的技术规范,占 49.71%。国际多采取 GPO+医院自行采购方式,更适合市场经济,贴近需求。其中,美国 GPO 发展时间最长,发展较为成熟。

4、投资标的
我国医疗器械行业迎来前所未有的发展良机,未来十年是国产创新医疗器械的黄金发展时期。从战略性的角度,我们做出这一判断主要基于三大理由:1、新需求和创新技术引领行业发展。2、进口替代加速和集中度提升催生龙头胜出。3、更好的融资环境和医疗政策驱动行业创新。从估值方法看,后续医疗器械板块中优质的产品管线,也会类似于创新药,开启 pipeline 估值法。
创新技术和新需求引领行业发展
从需求看,更微创、更精准、更早期诊断的器械需求在逐步增加。器械的创新需求和灵感很多来源于临床,中国巨大的手术量有助于持续挖掘出创新需求,目前国内频现自主创新的微创新类产品,例如艾德生物的基因检测产品、心脉医疗的术中支架、健帆生物血液灌流器、南微医学的牵引器等。从供给看,医院端“以药养医”模式在医疗政策推动下将逐步淡化,以医疗器械作为重要支撑的新医疗技术和医疗服务将会逐渐绽放更多光彩。从药械比看,全球 vs 中国,尚有很大提升空间。根据《中国医疗器械行业发展报告(2017)》,截至 2016 年底,我国药品和医疗器械人均消费额的比例仅为 1:0.35,远低于 1:0.7 的全球平均水平,更低于发达国家 1:0.98 的水平。展望未来,创新技术和新需求将引领医疗器械行业发展。

进口替代和集中度提升催生行业龙头
除了需求的增长,进口替代是未来医疗器械行业的另一个巨大红利。目前,国产医疗设备已逐步突破多项技术壁垒,已经基本实现进口替代(国产占比超过 50%)的细分领域包括:1)植入性耗材中的心血管支架、心脏封堵器、人工脑膜、骨科植入物中的创伤类产品等;2)大中型医疗设备中的监护仪、DR 等;3)体外诊断领域的生化诊断;4)家用医疗器械中的制氧机、血压计等。追溯我国已经实现进口替代的器械细分领域的成功经验,技术、品牌、性价比、渠道都是国产企业的制胜法宝,政策对于国产产品的支持也起到一定助推作用。

进口替代发生的临界点有以下几个观察指标:一是人才和技术水平达标,二是使用者的知识得到普及,三是渠道触达。国产企业实现进口替代的最佳路径是:进口产品做过重点学术推广但市占率相对较低、内资企业集中度较低、进口替代刚开始、行业内第一梯队暂未形成。内资企业选择在此时进入,做出技术上有竞争力的产品,辅以强大的营销推广能力,有望铸就品牌护城河。
技术是核心竞争力,进入第一梯队至关重要。国外的医疗器械以颠覆性产品、微创新产品为主,技术含量较高,且需要自己做学术推广。国内医疗器械研发模式可以大致分为两种,一种是类似于 me-too 或者 me-better 创新药,跟随进口器械,或在其基础上进行一定程度的改进,研发风险较低,而且进口产品已经在前期做了一定的学术推广工作;另一种是自主创新的微创新类产品,国内市场先前并没有进口产品。对于第二类产品,属于进口替代之外的投资逻辑,通过国内企业从零开始进行学术推广和市场教育,逐步提升产品的渗透率。器械的创新需求和灵感很多来源于临床,中国巨大的手术量有助于持续挖掘出创新需求,目前国内频现自主创新的微创新类产品。
我国医疗器械很多细分领域竞争格局属于分散竞争型,这种格局为我国国产企业进口替代创造了良好的条件。在进口替代刚开始,内资企业集中度较低,行业内第一梯队暂未形成时进入,做出技术上有竞争力的产品,辅以强大的营销推广能力,铸就品牌护城河,是国产企业实现进口替代的最佳路径。例如上海微创和乐普医疗在 2004 年左右进入心血管支架领域,当时强生、美敦力、波士顿科学、雅培都是我国心血管支架的重要厂商,彼此间不存在绝对优势;由于心血管行业本身规模较大,也为我国国产企业预留了一定的发展空间。而且外资企业已经在前期做好了用户教育工作,微创和乐普凭借自身先进的技术和产品的性价比优势,以及全面的营销渠道完成进口替代,形成国产第一梯队(微创、乐普、吉威),之后竞争格局便维持至今近 10 年很难被打破。
乘着分级诊疗、基层放量的东风,在国家政策不断向国产设备倾斜的大趋势下,中国将有望迎来国产设备繁荣发展的新阶段,预计未来五到十年又将有多个细分领域完成进口替代。国内龙头将享有行业高增速及进口替代的双重驱动,行业集中度提升,市场竞争格局重塑,这样的领域是器械领域投资的黄金细分,主要包括彩超、化学发光、内镜耗材、骨科耗材、心脑血管耗材等板块,在技术已经媲美进口产品后,目前正在逐步进口替代,是未来牛股诞生的重要细分领域。相关公司如彩超领域的迈瑞医疗、开立医疗;化学发光领域的迈瑞医疗、安图生物、新产业、迈克生物;内镜耗材的南微医学;骨科耗材如威高股份、大博医疗、爱康医疗、春立医疗、凯利泰、三友医疗;TAVR 领域的启明医疗、沛嘉医疗;主动脉和外周耗材领域的微创医疗、心脉医疗等。在这些领域,国产企业的份额目前主要集中在二级及以下的基层市场,在政策利好及技术进步的驱动下,国产企业将逐步扩大在三级医院的市场份额,形成细分行业内国产第一梯队。国内医疗器械集中度也有望不断提升,2017 年前全球 CR20=54.5%,中国 CR20=14.18%,随着行业规范和医疗政策中对于高端器械的鼓励+中低端器械的集采,行业龙头市占率将持续提升。

优质医疗器械品种有望实现管线估值
医疗器械的研发周期相对较快,研发风险也较低,优质医疗器械品种未来也可能类似创新药,实现管线估值。估值体系的变化有望推动医疗器械板块中具有Biotech 属性的公司(主要是港股 18A 和科创板新兴企业)走出新的估值提升行情,进而也会拉动现有医疗器械企业在研品种的价值重估。
推荐关注以下标的:
a) 医疗设备:迈瑞医疗、开立医疗、万东医疗、鱼跃医疗等;
b) 医用耗材:微创医疗(H)、乐普医疗、健帆生物、南微医学、心脉医疗、威高股份(H)、大博医疗、爱康医疗(H)、春立医疗(H)、凯利泰、三友医疗、先健科技(H)、启明医疗(H)、沛嘉医疗(H)等;
c) IVD:安图生物、新产业、迈克生物、艾德生物、万孚生物、凯普生物等。
……
(报告观点属于原作者,仅供参考。报告来源:兴业证券)
来源:兴业证券
关注我们的微信公众号
获得更多资讯


 京公网安备 11010502031898号
京公网安备 11010502031898号

